公司邮箱
contact@innermed.com
【专家笔谈】小肠疾病在超声内镜下的表现
文献来源:中华炎性肠病杂志,2024年第8卷第2期
作者:刘钟城1,2,3 美合日古丽·库尔班1,2,3 肖婷1,2,3 郭勤1,2,3,4
作者单位:1,4中山大学附属第六医院小肠内镜科;2广东省结直肠盆底疾病研究重点实验室;3广州市黄埔区中六生物医学创新研究院;4中山大学附属第六医院消化内科
通信作者:郭勤
引用本文: 刘钟城,美合日古丽·库尔班,肖婷,等. 小肠疾病在超声内镜下的表现[J]. 中华炎性肠病杂志(中英文),2024,08(02):132-136.DOI:10.3760/cma.j.cn101480-20230426-00069
【摘要】小肠疾病是目前消化界的研究热点。在小肠镜白光下检出病变后,可利用小肠超声内镜检查对病变层次进行评估,进而指导临床诊断与进一步治疗。本文归纳了各种小肠疾病在小肠超声内镜下的表现,以供参考。
【关键词】小肠超声内镜;小肠黏膜隆起;小肠溃疡;小肠狭窄
小肠病灶从形态上可分为隆起性病变、溃疡性病变、狭窄性病变及血管性病变等。小肠镜虽然能在白光下观察病变,但不能观察肠壁深层次的情况。超声内镜(endoscopic ultrasound,EUS)通过消化管腔,将超声探头直接贴于病变处,减小探头与病变的距离,避免肠道气体干扰,降低声衰减,提高分辨率,以获得肠腔各层次的组织学特征及周围邻近脏器的超声内镜图像 [ 1 ]。与经腹腔外超声相比,EUS可避免肠腔内气体及回声衰减的干扰,可以更为准确、完整地显示深部层次情况。对于隆起性病变,EUS可根据病变与肠道管壁的层次结构的关系,判断病变的大小、起源层次及回声特点,初步明确病变性质 [ 2 ]。对于溃疡性及狭窄性病变,白光内镜仅可见肠腔表面情况,不能了解深层次病变;EUS可以准确掌握肠壁层次及结构的改变,从而提高对溃疡性或狭窄性病变活动度评估的准确性 [ 3 ]。对于血管性病变,EUS可清晰显示血管与管壁层次的关系,可协助诊断并指导治疗 [ 4 ]。
在小肠超声内镜(small intestinal endoscopic ultrasound,SIEUS)下,小肠正常肠壁分6层,即第1层绒毛层、第2层黏膜层、第3层黏膜肌层、第4层黏膜下层、第5层固有肌层、第6层浆膜层,其回声从内向外呈高、高、低、高、低、高的特点 [ 5 ]。因受解剖位置等影响,既往EUS仅限于十二指肠降段及以上位置和回肠末端距回盲瓣20~30 cm及以下位置,余小肠无法探及。2000年,Watanabe等 [ 6 ]首次将SIEUS用于诊断小肠脂肪瘤患者。2006年,国内诸琦等 [ 7 ]通过对9例患者进行了小肠腔内超声探查,提示其对小肠黏膜下肿瘤的性质鉴别、早期克罗恩病(Crohn′s disease,CD)的诊断及肿瘤侵犯深度的判断存在一定作用。2007年日本Fukumoto等 [ 8 ]对20例患者进行双气囊小肠镜联合EUS检查,7例检出隆起性病变,7例检出溃疡性病变,均取得了理想的结果。因此,SIEUS可很好地明确隆起性病变、溃疡性病变、狭窄性病变及血管性病变的大小、起源及回声特点,从而辅助临床诊断及治疗。本文就小肠疾病在SIEUS下的表现作一简述。
一、SIEUS在隆起性病变中的表现
小肠隆起性病变是消化道上皮下病变,属于一类来源于非黏膜层的肿物。对于小肠隆起性病变,既往只能根据肠道超声、计算机体层成像(computed tomograph,CT)或磁共振成像(magnetic resonance imaging,MRI)检查来确定,但这些检查无法判断部分病变是来源于腔内还是腔外。SIEUS可以准确地判断病变部位及其与消化管壁的关系、病变大小、起源层次,并根据内部回声强弱、均匀与否、边缘清晰程度、与周围脏器关系、浸润深度及周围淋巴结情况等综合判断病变性质,从而决定下一步治疗方式。目前暂无小肠隆起性病变SIEUS特点的诊断标准,根据笔者中心经验及既往文献复习,主要特点如下。
1.小肠癌:小肠镜下表现为菜花样、隆起性肿物,表面溃烂,覆厚污苔。SIEUS下表现为肠壁层次破坏,呈不均匀低回声改变,可出现浆膜层突破 [ 7 ]。
2.小肠间质瘤:小肠镜下表现为半球样黏膜隆起,部分表面光滑,部分表面充血糜烂,表面凹陷伴溃疡形成( 图1A )。SIEUS下病变呈均匀的低回声改变,边界较清晰,多呈类圆形,大多数来源于固有肌层,也可起源于黏膜肌层 [ 8 , 9 , 10 ]( 图1B )。
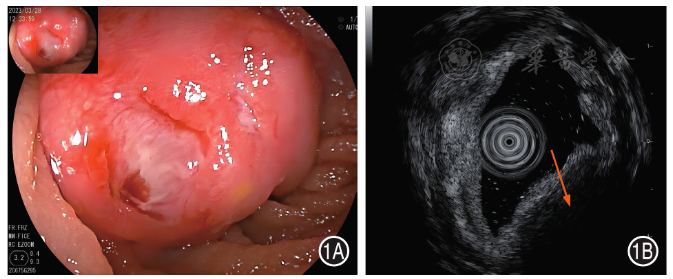
图1 小肠间质瘤患者小肠镜和小肠超声内镜图 1A:小肠镜示空肠下段一黏膜隆起,表面见溃疡形成;1B:小肠超声内镜示起源于固有肌层的低回声病变(箭头)
3.小肠平滑肌瘤:小肠镜下形态多呈半球形或长条形隆起,表面多光滑,少部分表面可有充血糜烂,活动度较好。SIEUS下示类圆形低回声团块,边界清晰,源于黏膜肌层或固有肌层,内部回声均匀。
4.小肠异位胰腺:小肠镜下表现为实性结节样改变,表面光滑,黏膜表面可出现脐样凹陷的导管开口( 图2A )。SIEUS下多呈中、高回声,内部可有点状高回声,来源于黏膜下层或黏膜肌层,其内部有无回声腺管状结构,边界清晰,后方固有肌层增厚 [ 10 ]( 图2B )。
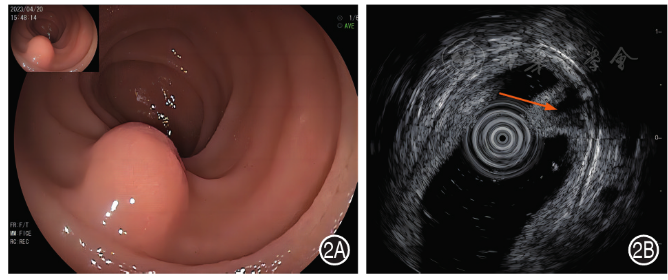
图2 小肠异位胰腺患者小肠镜和小肠超声内镜图 2A:小肠镜示回肠上段一黏膜隆起,表面似见一开口;2B:小肠超声内镜示起源于黏膜肌层的高回声病变,中央见一无回声的腺管样结构(箭头)
5.小肠神经内分泌肿瘤:小肠镜下呈广基或亚蒂隆起性病变,边界清晰,表面呈淡黄色或白色,触之较硬。SIEUS下为均匀的低回声病灶,边界光滑清晰,多位于黏膜肌层或黏膜下层,其低回声比黏膜肌层或固有肌层的低回声稍高 [ 10 ]。
6.小肠脂肪瘤:小肠镜下呈表面光滑的球样隆起,表面光滑,黏膜可见黄色外观。SIEUS下显示圆形或卵圆形高回声团块影,起源于黏膜下层,边缘清晰,内部回声均匀 [ 6 ]。
7.小肠囊肿:小肠镜下表现为表面光滑、可压缩、触之可滑动的隆起。SIEUS下表现为类圆形无回声改变,边界清楚,部分囊肿内部可见分隔状回声,多起源于黏膜层或黏膜下层。
8.黑斑-息肉综合征(Peutz-Jeghers syndrome,PJS)及Cronkhite-Canada综合征(CCS):PJS及CCS在小肠镜下表现为带蒂或亚蒂息肉。SIEUS下表现为类圆形的均匀中高回声改变,边界清晰,来源于黏膜层。SIEUS可扫查息肉周围血管,若息肉旁有粗大血管,可进行预防性钛夹夹闭止血,减少术中或术后出血风险。
二、SIEUS在溃疡性及狭窄性病变中的表现
在临床中,对于溃疡性及狭窄性病变,多采用肠道超声、CT或MRI来评估炎症反应的情况,但这些检查受患者检查前准备的影响,无法准确评估全小肠病变。SIEUS可对病变进行靶向超声。在SIEUS的评估中,可根据肠壁炎症反应深度和肠壁总厚度来综合评估其活动性变化,这有利于疾病诊断及病情评估与预后预估,为选择合适的治疗方法提供依据。而且,目前SIEUS在小肠溃疡性及狭窄性病变领域的应用,已从基本的病情评估转变为病情预后判断和指导后续用药。因小肠狭窄发生时多合并溃疡,故本文把溃疡性病变和狭窄性病变合并总结。目前暂无小肠溃疡性及狭窄性病变SIEUS特点的诊断标准,根据笔者中心经验及既往文献复习,主要特点如下。
1.小肠CD:CD的小肠镜下表现为偏心性或向心性狭窄,以及纵行、不规则或阿弗他溃疡( 图3A )。SIEUS下病灶处肠壁全层呈不同程度增厚,以黏膜下层或固有肌层增厚为主,且黏膜下层呈稍高或稍低回声改变,层次可辨但分界多欠清,溃疡处可见前两层肠壁结构消失( 图3B )。缓解期溃疡瘢痕处肠壁无明显增厚 [ 9 , 11 , 12 ]。
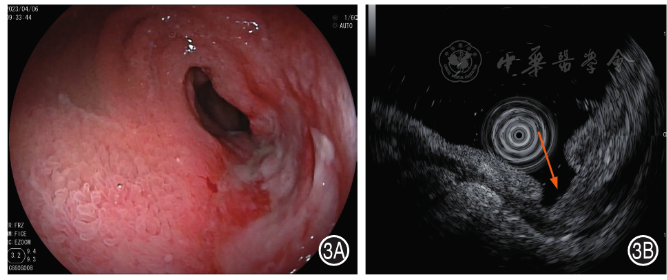
图3 小肠克罗恩病患者小肠镜和小肠超声内镜图 3A:小肠镜示空肠下段纵行溃疡,溃疡表面覆白苔,溃疡周围充血水肿;3B:小肠超声内镜示溃疡处黏膜层及黏膜肌层缺失,溃疡周围肠壁全层增厚,以黏膜下层增厚为主(箭头)
2.小肠结核:小肠镜下表现为环行或鼠咬状溃疡,溃疡表面覆白苔,溃疡周围黏膜呈鼠咬状( 图4A )。SIEUS下显示溃疡处黏膜层缺失,病灶周边肠壁稍增厚,以固有肌层增厚为主,且黏膜下层变窄、回声减弱 [ 9 , 13 ],但肠壁全层不一定增厚,甚至可能变薄,这可能与疾病消耗相关( 图4B )。
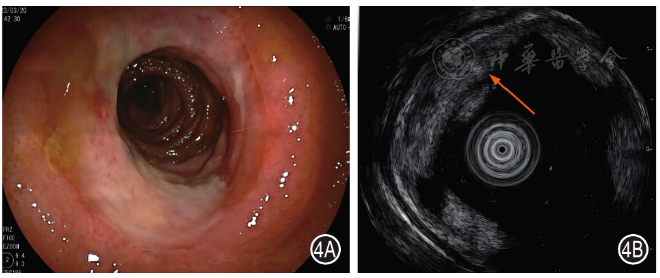
图4 小肠结核患者小肠镜和小肠超声内镜图 4A:小肠镜示回肠上段见片状溃疡,溃疡表面覆白苔;4B:小肠超声内镜示溃疡处黏膜层缺失,溃疡周围肠壁增厚,以固有肌层增厚为主(箭头)
3.小肠白塞病:小肠镜下表现为圆形、椭圆形或不规则溃疡,溃疡多深大,边界清晰,溃疡之间黏膜正常,病变不连续( 图5A )。SIEUS显示肠壁层次结构模糊,肠壁全层增厚,以黏膜下层及固有肌层增厚为主,黏膜下层呈稍低回声改变( 图5B )。
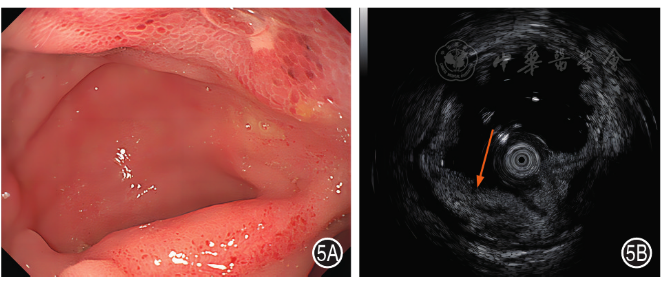
图5 小肠白塞病患者小肠镜和小肠超声内镜图 5A:小肠镜示回肠末端不规则凹陷性溃疡,溃疡面覆白苔,溃疡周围黏膜充血;5B:小肠超声内镜示肠壁层次结构模糊,肠壁全层增厚,以黏膜下层及固有肌层增厚为主(箭头)
4.小肠淋巴瘤:小肠镜下的表现没有特征性,主要表现为不规则溃疡、隆起性肿块、滤泡样增生( 图6A )。SIEUS下表现为黏膜下层增厚、呈低回声改变,随着疾病进展可出现肠壁层次的融合、肠壁结构消失,部分突破浆膜层 [ 9 , 14 ]( 图6B )。
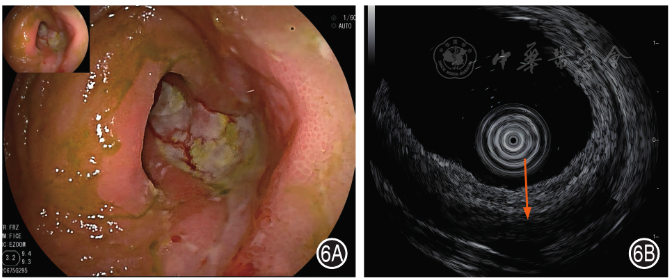
图6 小肠淋巴瘤患者小肠镜和小肠超声内镜图 6A:小肠镜示回肠中段见纵行溃疡,溃疡表面覆白苔;6B:小肠超声内镜示肠壁全层增厚,以黏膜下层及固有肌层增厚为主,肠壁分界部分欠清(箭头)
5.隐源性多灶性溃疡性狭窄性小肠炎(cryptogenic multifocal ulcerous stenosing enteritis,C-MUSE):C-MUSE在小肠镜下表现为多发浅表溃疡和肠腔狭窄( 图7A )。SIEUS下显示肠壁全层增厚,以黏膜层及黏膜肌层增厚为主,黏膜下层也有增厚,固有肌层一般不增厚,各层次结构清晰( 图7B )。
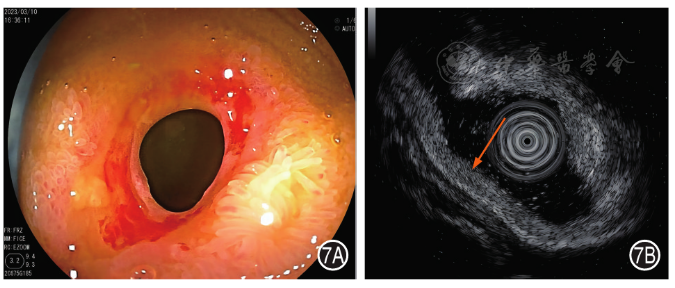
图7 隐源性多灶性溃疡性狭窄性小肠炎患者小肠镜和小肠超声内镜图 7A:小肠镜示回肠中段一环形狭窄,狭窄周围未见溃疡形成,小肠镜无法通过;7B:小肠超声内镜示肠壁全层增厚,以黏膜层及黏膜肌层增厚为主,各层次结构清晰(箭头)
首先,需要判断狭窄性质。若小肠狭窄处的肠壁黏膜层、黏膜下层呈低回声,则为炎性充血水肿,使用生物制剂及免疫抑制剂可以缓解狭窄。若小肠狭窄处的肠壁黏膜层、黏膜下层是高回声,则为纤维性狭窄,生物制剂及免疫抑制剂较难缓解狭窄,需小肠镜下切开或者扩张治疗。其次,对于小肠纤维性狭窄患者,若SIEUS评估黏膜层或黏膜肌层增厚,则可进行小肠镜下切开或扩张治疗;若黏膜下层或固有肌层增厚,小肠镜下切开或扩张具有较高的穿孔风险,应进行药物治疗后再行小肠镜下治疗。Wada等 [ 15 ]通过SIEUS评估小肠狭窄程度,其中4例患者病变未累及固有肌层及浆膜层,行小肠镜下球囊扩张后未出现并发症;另外2例患者肠壁5层结构被破坏,未行内镜下球囊扩张。
三、SIEUS在血管性病变中的表现
小肠血管性病变是小肠出血的三大病因之一。行SIEUS寻找病变来源层次及起源血管,可更精准地进行相应小肠镜下治疗,如氩离子凝固术、硬化剂注射治疗、金属夹夹闭、黏膜下注射肾上腺素等。此外,还可以评估黏膜下药物注射的治疗情况。
1.小肠血管瘤:小肠镜下见紫红色黏膜隆起,表面光滑( 图8A )。SIEUS下表现为管壁外无回声或低回声圆形结构,追溯起源,是由邻近血管部分扩张所致 [ 10 ]。若合并纤维化,也可呈等回声或偏高回声改变( 图8B )。小肠镜下硬化治疗或圈套治疗均有较好疗效。
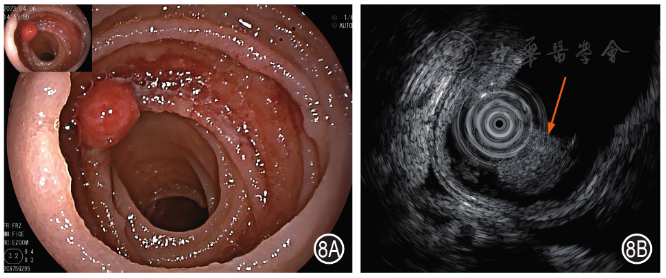
图1 小肠间质瘤患者小肠镜和小肠超声内镜图 1A:小肠镜示空肠下段一黏膜隆起,表面见溃疡形成;1B:小肠超声内镜示起源于固有肌层的低回声病变(箭头)
2.小肠淋巴管瘤:小肠镜下为白色或浅黄色的透明肿块,突入管腔,表面黏膜多光滑、完整( 图9A )。SIEUS下多起源于黏膜层及黏膜下层,内部呈均匀低回声,伴管状结构,边界清晰 [ 10 ]( 图9B )。一般淋巴管瘤无需治疗,若合并出血或出现梗阻症状,可采取手术切除、穿刺抽吸、硬化疗法、激光等方法进行治疗。小肠镜下注射聚桂醇有较好效果,注射治疗后行SIEUS,可准确评估注射是否成功。SIEUS下提示无回声、有边界团块影,表示注射成功( 图9C )。
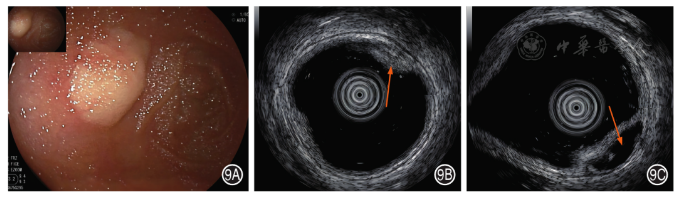
图9 小肠淋巴管瘤患者小肠镜和小肠超声内镜图 9A:小肠镜示空肠中段一黏膜隆起,表面光滑,呈淡黄色;9B:小肠超声内镜示来源于黏膜层的等回声病变,余层次清晰(箭头);9C:小肠超声内镜示注射聚桂醇治疗后原病变处呈无回声改变(箭头)
3.小肠血管畸形:大部分小肠出血患者小肠镜下表现为搏动的出血点,即小肠某一处渗血,且伴有搏动,其本质为小肠血管畸形。行SIEUS检查追踪其起源血管,一般表现为无回声管腔样结构,追溯起源可见由管壁腔外血管穿行入壁,部分未见血管变小。对此,可进行小肠镜下硬化治疗、金属夹夹闭治疗或氩离子凝固术等。
4.小肠蓝色橡皮疱痣综合征:小肠镜下表现为蓝紫色乳头状或丘疹样隆起。SIEUS下为来源于黏膜下层的类圆形、无回声结构。
四、总结
综上所述,各种小肠疾病在SIEUS下具有不同的表现特点,SIEUS弥补了小肠镜检查仅能观察消化道黏膜层病变,而不能对黏膜深层的状况进行观察的不足,有助于判断小肠黏膜下肿物的来源层次、切面大小及回声特点;也有助于做好小肠溃疡性及狭窄性病变的诊断与鉴别诊断、评估疾病的活动度和严重程度、预测复发及诊断相关并发症;更有助于指导小肠血管性病变的治疗等。
但目前国内外开展SIEUS的中心较少,还处于初步探索阶段,且对小肠镜操作医师的技术及临床诊断要求较高,比如由于小肠蠕动较快,小肠腔内无法长久保持良好的水充盈状态,因此使用三通或头端带水囊的小探头超声会更有利于病灶的探查。未来随着小肠镜医师技术和医疗器械的不断精进,SIEUS将在小肠疾病诊断和治疗中发挥越来越重要的作用。
利益冲突 所有作者均声明不存在利益冲突
参考文献略
本刊刊发文章可通过中华医学期刊网下载阅读
本文版权归《中华炎性肠病杂志》所有
文章转载来源:中华炎性肠病杂志公众号